Todo lo que debe saber sobre los tratamientos para modificar el ADN
La terapia génica ha sido noticia en los últimos años, en parte debido al rápido desarrollo de la biotecnología que permite a los médicos administrar estos tratamientos. En términos generales, las terapias génicas son técnicas utilizadas para tratar o prevenir enfermedades modificando el contenido o la expresión del ADN de las células, a menudo sustituyendo genes defectuosos por otros funcionales.
El término "terapia génica" aparece a veces junto a información errónea sobre las vacunas de ARNm, que incluyen las vacunas COVID-19 de Pfizer y Moderna. Estas vacunas contienen ARNm, un primo genético del ADN, que incita a las células a fabricar la "proteína pico" del coronavirus. Las vacunas no alteran el ADN de las células y, tras fabricar la espiga, las células descomponen la mayor parte del ARNm. Otras vacunas COVID-19 incluyen las vacunas de vector vírico fabricadas por AstraZeneca y Johnson & Johnson, que introducen ADN en las células para obligarlas a fabricar proteínas de espiga. Las células que fabrican estas proteínas, siguiendo las instrucciones del ARNm o de las vacunas de vectores virales, sirven de diana para el sistema inmunitario, por lo que no permanecen mucho tiempo en el organismo. Esto es muy, muy diferente de la terapia génica, cuyo objetivo es cambiar la función de las células a largo plazo.
Veamos en qué consiste la terapia génica y respondamos a algunas de las preguntas más frecuentes.
Todo lo que debe saber sobre los cálculos renales
Todo lo que debe saber sobre el insomnio
Qué es la terapia génica y qué hace con el ADN?
El ADN es una molécula que almacena información genética, y los genes son fragmentos de información genética que las células utilizan para fabricar un producto concreto, como una proteína. El ADN se encuentra en el núcleo de la célula, donde está empaquetado en cromosomas, y también en las mitocondrias, los orgánulos "centrales" situados fuera del núcleo.
Aunque hay enfermedades mitocondriales que algún día podrían curarse con terapia génica, actualmente el término terapia génica se refiere a tratamientos dirigidos a genes nucleares, es decir, los genes de los 23 pares de cromosomas del interior del núcleo.
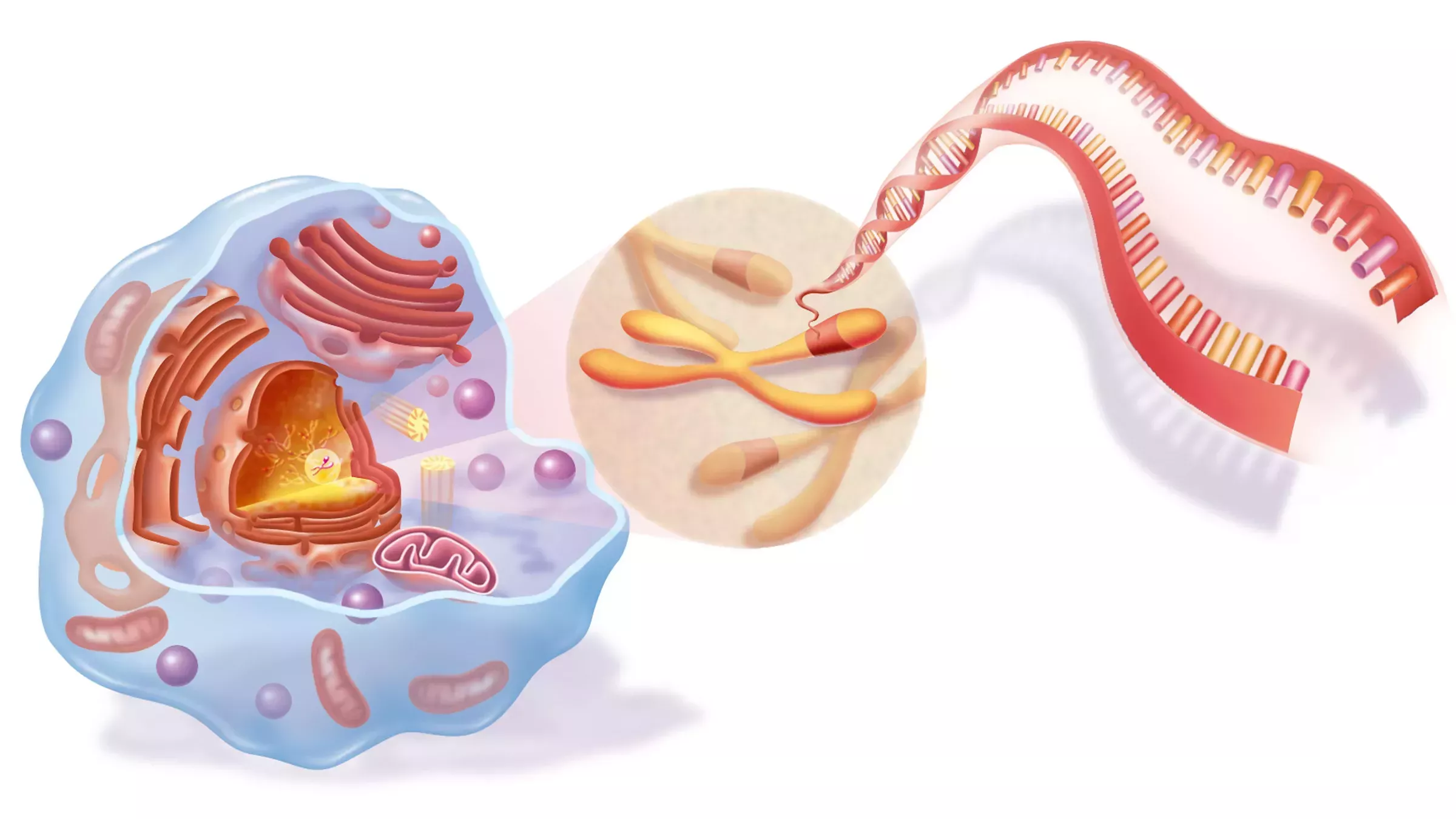
Clásicamente, la terapia génica se ha referido al proceso de "eliminar" un gen disfuncional o añadir una copia de un gen funcional al núcleo para mejorar la función celular. En la actualidad, la terapia génica se dirige a enfermedades derivadas de un problema con un solo gen, o a lo sumo unos pocos genes, más que a las que afectan a muchos genes.
Sin embargo, el campo de la terapia génica se está ampliando para incluir estrategias que no entran en las categorías clásicas de eliminar genes malos o añadir genes buenos. Por ejemplo, los investigadores de Sangamo Therapeutics están desarrollando técnicas genéticas para tratar las enfermedades de Parkinson, Alzheimer y Huntington que actúan aumentando o suprimiendo la actividad de genes específicos.
Aunque los tratamientos pueden añadir genes a las células del cuerpo, eliminar genes o actuar de algún modo para cambiar la función de los genes, cada terapia génica se dirige a las células de tejidos corporales concretos. Por lo tanto, cuando los científicos y los médicos hablan de lo que la terapia génica hace con el ADN, no se refieren a todo el ADN del cuerpo, sino sólo a una parte.
¿Cómo funciona la terapia génica?
La terapia génica puede ser ex vivo o in vivo.
La terapia génica ex vivo consiste en extraer células del organismo, tratarlas y devolverlas al cuerpo. Este es el método utilizado para tratar enfermedades genéticas de las células sanguíneas, porque se puede extraer médula ósea del paciente, tratar células madre de esa médula con terapia génica -por ejemplo, para aportar un gen que falta o no funciona correctamente- y volver a infundir al paciente las células transformadas.
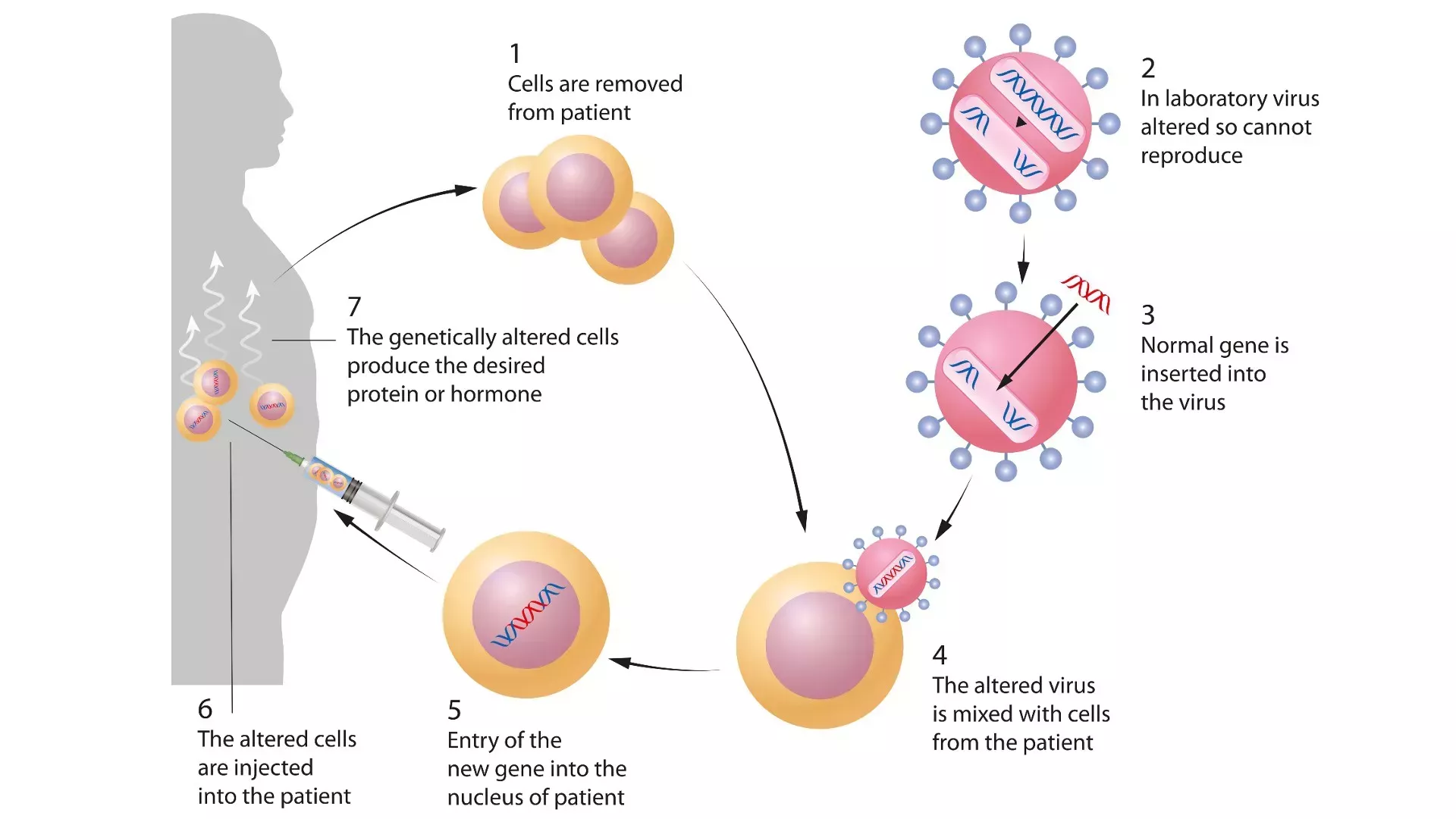
La terapia génica in vivo significa que la propia terapia génica se inyecta o infunde en la persona. Esto puede hacerse mediante inyección directa en el lugar anatómico donde se necesita la terapia génica (un ejemplo común es la retina del ojo), o puede significar la inyección o infusión de una carga genética que debe viajar a los tejidos corporales donde se necesita.
Tanto en la terapia génica ex vivo como en la in vivo, la carga genética se empaqueta en un contenedor, denominado vector, antes de introducirla en las células o en el organismo. Uno de estos vectores es el virus adenoasociado (AAV). Se trata de un grupo de virus que existen en la naturaleza pero a los que se han eliminado sus genes habituales y se han sustituido por una carga genética, lo que los convierte en vectores de terapia génica.
¿Es segura la terapia génica?
El AAV se ha utilizado durante muchos años para administrar terapia génica porque tiene un buen historial de seguridad. Es mucho menos probable que provoque una respuesta inmunitaria peligrosa que otros virus que se utilizaban como vectores hace varias décadas, cuando la terapia génica estaba dando sus primeros pasos. Además, el empaquetado de cargas genéticas en portadores AAV permite que la terapia génica inyectada o infundida se desplace a los tejidos corporales concretos donde se necesita. Esto se debe a que hay muchos tipos de AAV, y ciertos tipos se sienten atraídos por determinados tejidos u órganos. Así, si una carga genética debe llegar a las células hepáticas, por ejemplo, se puede empaquetar en un tipo de AAV al que le guste ir al hígado.
En los primeros tiempos de la terapia génica, que comenzó en 1989, los investigadores utilizaban retrovirus como vectores. Estos virus introducían una carga genética directamente en los cromosomas nucleares del paciente. Sin embargo, existía el temor de que la integración de nuevo ADN en los cromosomas pudiera provocar cambios que dieran lugar a cáncer (se abre en una nueva pestaña), por lo que la estrategia se abandonó en un principio. (Más recientemente, los científicos han utilizado con éxito retrovirus en terapias génicas experimentales sin causar cáncer; por ejemplo, se utilizó una terapia basada en retrovirus para tratar a bebés con la "enfermedad del niño burbuja").

Tras alejarse de los retrovirus, los investigadores recurrieron a los adenovirus, que ofrecían la ventaja de entregar la carga genética en forma de episoma, un fragmento de ADN que funciona como un gen dentro del núcleo, pero que permanece como una entidad separada de los cromosomas. El riesgo de cáncer era extremadamente bajo con esta innovación, pero los vectores de adenovirus resultaron estimular el sistema inmunitario de forma muy poderosa. En 1999, una reacción inmunitaria a la terapia génica con adenovirus provocó la muerte de Jesse Gelsinger, un joven de 18 años que se había presentado voluntario para un ensayo clínico.
La muerte de Gelsinger conmocionó a la comunidad de la terapia génica, paralizando el campo durante varios años, pero las terapias génicas actuales que han surgido a lo largo de los años basadas en AAV no son peligrosas. Sin embargo, suelen ser caras y el porcentaje de éxito varía, por lo que suelen utilizarse como último recurso para un número creciente de enfermedades genéticas.
¿Qué afecciones se tratan actualmente con terapia génica?
La terapia génica puede tratar determinadas enfermedades de la sangre, como la hemofilia A, la hemofilia B, la anemia falciforme y, a partir de 2022, la beta talasemia (se abre en una nueva pestaña). Lo que estas enfermedades tienen en común es que el problema se reduce a un solo gen. Por ello, la beta talasemia y la anemia falciforme se prestan a las terapias génicas ex vivo, que consisten en extraer y modificar células madre de la médula ósea, mientras que la hemofilia A y la hemofilia B se tratan con terapias génicas in vivo dirigidas a las células hepáticas. Dicho esto, existen otros tratamientos para estas enfermedades de la sangre, por lo que la terapia génica es más bien un último recurso.
Numerosos trastornos por deficiencia enzimática también se reducen a un gen defectuoso que hay que sustituir. La adrenoleucodistrofia cerebral, que provoca la acumulación de ácidos grasos en el cerebro, es uno de estos trastornos que puede tratarse con terapia génica, según el Hospital Infantil de Boston (se abre en una nueva pestaña). La terapia con células T CAR, que está aprobada para ciertos tipos de cáncer, consiste en extraer y modificar las células inmunitarias del paciente y se conoce como "terapia génica basada en células." (se abre en una nueva pestaña)
La terapia
génica
también ha sido útil para tratar enfermedades hereditarias de la retina (se abre en una nueva pestaña), para las que otros tratamientos no han sido útiles.¿Qué terapias génicas están en desarrollo?
Otro grupo de dianas para la terapia génica son las enfermedades del sistema nervioso.
"Nos encontramos en un momento extraordinario de las neurociencias, en el que se están desarrollando tratamientos para formas genéticas de trastornos neurológicos", declaró a Live Science la Dra. Merit Cudkowicz (se abre en una nueva pestaña), jefa de neurología del Hospital General de Massachusetts y profesora de la Facultad de Medicina de Harvard.
Por ejemplo, se están desarrollando terapias génicas para tratar un par de enfermedades genéticas llamadas enfermedad de Tay-Sachs y enfermedad de Sandhoff. Ambas enfermedades se deben a que unos orgánulos llamados lisosomas se llenan de unas moléculas parecidas a la grasa llamadas gangliósidos. Los efectos de estas enfermedades (se abre en una nueva pestaña) incluyen retraso en el desarrollo, pérdida de habilidades adquiridas, rigidez, ceguera, debilidad y falta de coordinación, con parálisis final. Los niños que nacen con la enfermedad de Tay-Sachs y la enfermedad de Sandhoff no suelen superar los 2 o 5 años de edad.
"No ha habido ninguna prueba prenatal o neonatal rutinaria para Tay-Sachs y Sandhoff, porque no ha habido ningún tratamiento disponible", afirma el Dr. Jagdeep Walia (se abre en una nueva pestaña), genetista clínico y jefe de la División de Genética Médica del Departamento de Pediatría y del Centro de Ciencias de la Salud de Kingston y la Universidad Queen's de Ontario (Canadá). Walia está desarrollando una terapia génica destinada a sustituir el gen de la Hex A, la enzima deficiente en estos niños. Hasta ahora, el tratamiento ha demostrado una buena eficacia y seguridad en modelos animales, pero aún debe probarse en pacientes humanos.
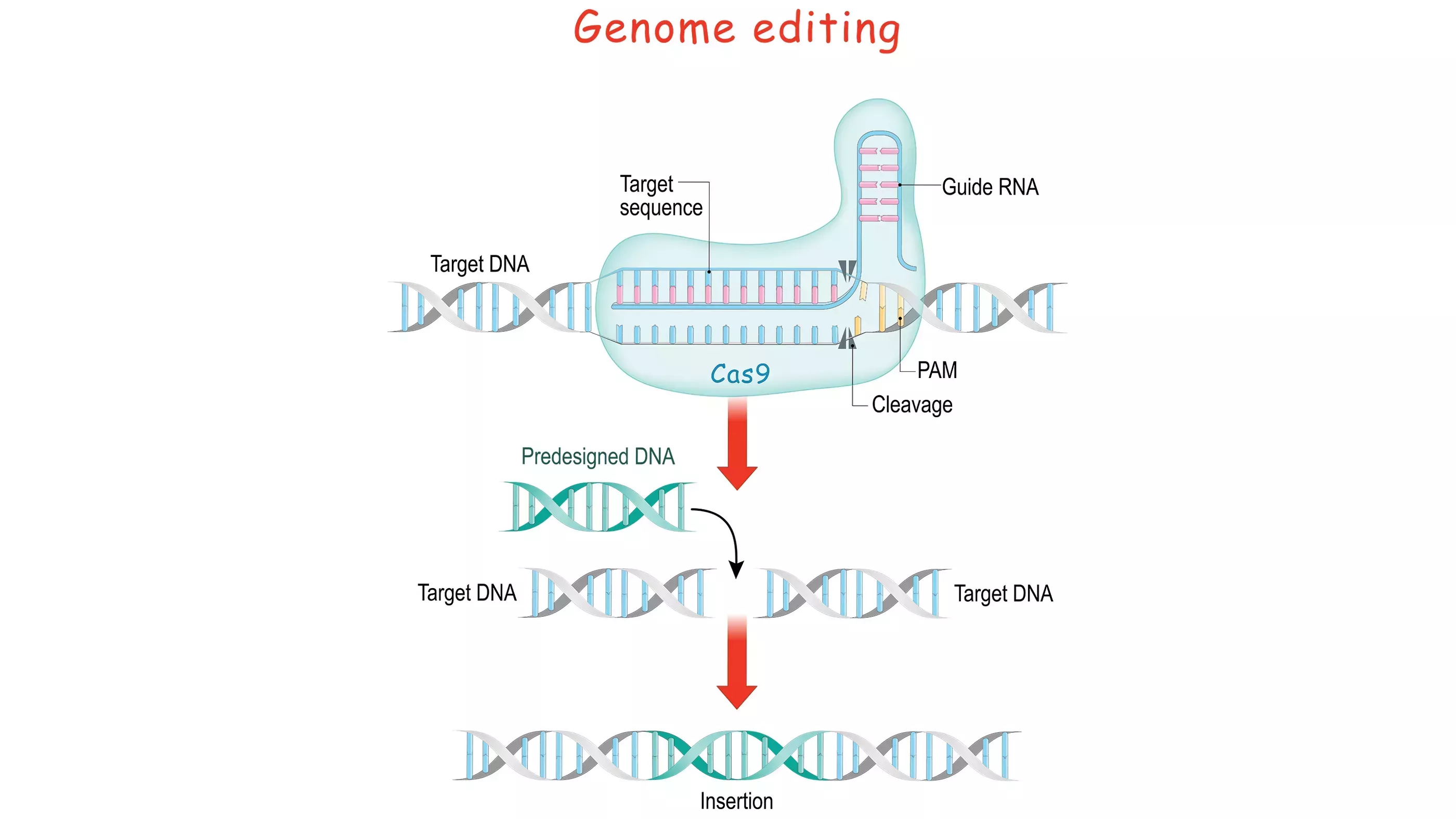
El futuro de la terapia génica en general parece esperanzador gracias a los nuevos avances tecnológicos, como la edición génica CRISPR. Se trata de una técnica extremadamente potente para cortar partes de moléculas de ADN e incluso pegar otras nuevas, de forma análoga a lo que se hace con el texto en las aplicaciones de tratamiento de textos. CRISPR no es el primer método utilizado por los científicos para editar el ADN, pero es mucho más versátil que otras técnicas. Aún no está listo para la manipulación cromosómica in vivo, pero avanza exponencialmente.




